Absorption et émission de photons par les atomes
Les atomes interagissent avec la lumière d'une manière étonnamment précise. Chaque fois qu'un électron change de niveau d'énergie, l'atome peut absorber ou émettre un photon. Ces processus sont au cœur de la physique quantique et expliquent une grande partie du comportement de la matière.
Rappel essentiel
Dans un atome décrit par la mécanique quantique, les électrons ne circulent pas librement autour du noyau. Ils occupent des niveaux d'énergie bien définis, associés à des orbitales aux formes et orientations caractéristiques.
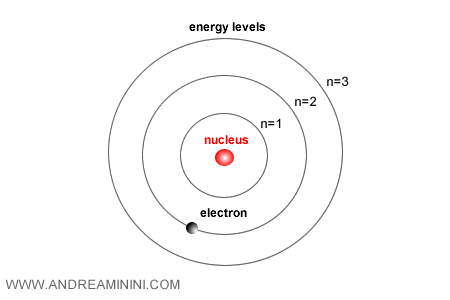
Plus un niveau est proche du noyau, plus son énergie est faible. Les niveaux plus éloignés sont plus énergétiques.
Cette structure en niveaux permet de comprendre comment et pourquoi la lumière peut être absorbée ou émise.
Absorption d'un photon
Lorsqu'un atome est exposé à un rayonnement électromagnétique, certains photons peuvent interagir directement avec ses électrons.
Si l'énergie d'un photon correspond exactement à la différence entre deux niveaux d'énergie, l'électron peut l'absorber. Il gagne alors de l'énergie et passe à un niveau supérieur.
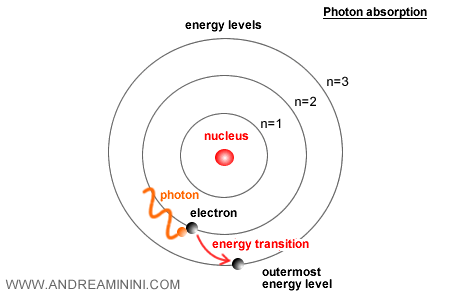
Électron excité. Un électron est dit excité lorsqu'il a absorbé de l'énergie et occupe un niveau plus élevé que son état habituel.
Si l'énergie absorbée dépasse l'écart entre les niveaux, l'électron peut carrément quitter l'atome.
Ionisation. Si l'énergie absorbée est supérieure à l'énergie d'ionisation, l'électron est arraché à l'atome, qui devient alors un ion positif.
Émission d'un photon
Un électron excité ne reste pas longtemps dans cet état. Au bout d'un temps très court, il redescend spontanément vers un niveau plus bas.
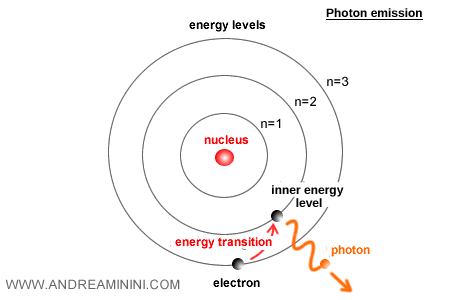
Toute baisse d'énergie doit être compensée. Lors de la transition descendante, l'électron libère l'énergie excédentaire sous forme de photon.
L'énergie du photon émis correspond exactement à la différence entre les niveaux d'énergie. Une fois cette énergie évacuée, l'électron retrouve son état fondamental.
Note. Les électrons ne peuvent pas se déplacer continuellement vers le noyau. Ils ne peuvent occuper que des niveaux bien définis, appelés états stationnaires. Ils passent de l'un à l'autre en émettant ou absorbant une quantité d'énergie précise. Ce principe constitue l'une des bases de la mécanique quantique et du modèle de Bohr.
Un photon est émis uniquement lors d'une transition descendante.
Tant qu'un électron reste dans un état stationnaire, il ne rayonne aucune énergie.